据悉,北京科技大学的海明潭教授,上海交通大学附属第六人民医院朱悦琦主任和美国三院院士,哈佛大学的David A. Weitz教授通过微流控技术创建出了一种非常高效的纳米给药体系。通过这个纳米药物传递体系实现分子靶向药物和化学药物的多药联用,在低剂量静脉注射的情况下,就可以抑制人类表皮因子受体2阳性乳腺肿瘤达到90%。这一******研究成果在线发表于知名学术期刊PNAS上。与传统工艺相比,微流体技术可以极大的改善生产粒子的均一性,极大的提高药物的装载效率,并可以实现高通量的工业化生产。
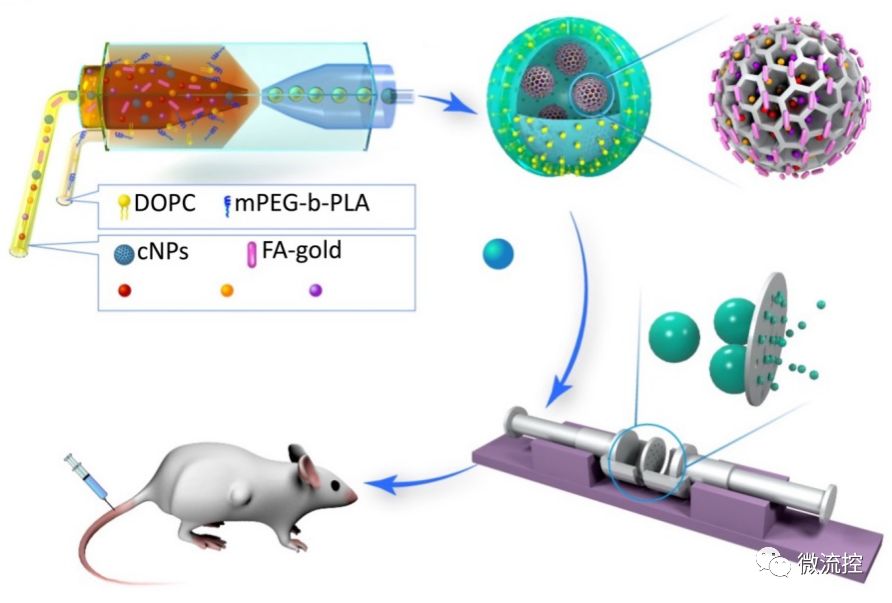
科研人员提出微流体双乳体系,从而非常高效的实现封装多种疏水性及亲水性物质。介孔硅纳米粒子有非常好的生物相容性、生物可降解性、高载药率及表面可功能化修饰等特点。而金纳米粒子在生物成像及光热治疗方面被广泛应用。在该项目中,该研究团队首先把金纳米棒通过化学反应结合在介孔硅表面,然后通过介孔硅装载大量亲水、疏水、蛋白及核酸药物,并通过微流体双乳法一步将介孔硅包裹在了以高分子为主体,同时复合磷脂的巨型囊泡中。随后,基于过膜挤压的调控,构建出了多药物同时负载的纳米载药粒子。
该纳米载药体系在HER2阳性乳腺癌小鼠模型中得到了验证。该纳米体系有非常好的生物相容性,并可以在肿瘤中长时间驻留。通过连续注射该纳米体系,小鼠的肿瘤抑制率超过了90%,而且该体系极大的降低了癌细胞的耐药性及药物引起的副作用。
因为这个纳米体系具有普适性,这个方法将有可能被广泛应用到其他类型癌症及其他类型疾病的治疗上。而且因为制备方法简单有效,研究团队认为该方法有临床转化的潜力。希望研究团队带来的纳米载药新体系,最终可以帮助更多癌症患者改善预后。
本文转自:电子发烧友网,如有侵权联系删除